中国医疗器械UDI详解
医疗器械是医疗体系中不可或缺的重要组成部分,其安全性和可追溯性对于患者健康至关重要。为加强医疗器械监管,中国国家药品监督管理局(NMPA)推行了医疗器械唯一标识(Unique Device Identification,UDI)系统。本文将详细解释UDI的概念、组成、实施意义、在中国的推行进展以及相关挑战。
一、UDI的概念与组成
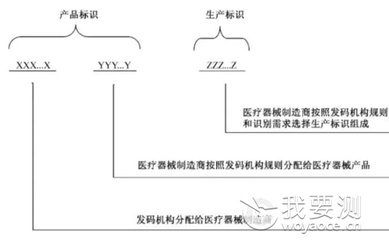
医疗器械唯一标识(UDI)是一种全球通用的标准化系统,用于唯一识别医疗器械产品。它类似于商品的条形码或二维码,但专为医疗器械设计,旨在实现产品的全生命周期追溯。UDI由两个主要部分组成:设备标识符(DI)和生产标识符(PI)。
- 设备标识符(DI):这是UDI的静态部分,用于识别特定医疗器械的制造商、型号和版本等信息。它相当于产品的“身份证”,在全球范围内唯一。
- 生产标识符(PI):这是UDI的动态部分,包含生产相关信息,如批号、序列号、生产日期和有效期等。这有助于追踪具体批次或单个产品。
UDI通常以数据载体形式呈现,如二维码或RFID标签,便于扫描和记录。
二、UDI在中国的实施意义
UDI系统的引入对中国的医疗器械行业具有深远影响:
- 提升可追溯性:UDI允许从生产、流通到使用环节的全程追踪,一旦发生质量问题或不良事件,能快速定位和召回产品,保障患者安全。
- 加强监管效率:监管部门可通过UDI数据库(如中国医疗器械唯一标识数据库)实时监控产品流向,减少假冒伪劣产品流入市场,提高监管精准度。
- 促进产业规范化:UDI要求企业采用标准化编码(如GS1标准),推动医疗器械生产和管理流程的数字化和自动化,降低错误率,提升运营效率。
- 支持医疗创新:UDI数据可用于分析和研究,帮助识别产品性能趋势,为政策制定和产品改进提供依据。
三、中国UDI的推行进展
中国于2019年启动UDI试点工作,并于2021年正式发布《医疗器械唯一标识系统规则》,分阶段强制实施。目前,UDI已覆盖高风险医疗器械(如植入物、体外诊断试剂等),并逐步扩展到其他类别。企业需在产品和包装上标注UDI,并向国家数据库上报相关信息。相关部门如NMPA和卫生健康委员会协同推进,确保UDI与医院信息系统(如电子病历)对接,实现临床应用。
四、实施挑战与未来展望
尽管UDI带来诸多益处,但实施过程中仍面临挑战:中小企业可能因成本和技术问题难以适应;数据整合需要跨部门协作;部分医疗机构缺乏配套基础设施。未来,中国将进一步完善UDI法规,推广云计算和物联网技术,实现UDI与全球标准接轨,最终构建一个高效、透明的医疗器械生态系统。
UDI是医疗器械监管的重要工具,它不仅提升了产品安全,还推动了行业数字化转型。随着中国医疗体系的不断完善,UDI将在保障公众健康方面发挥更大作用。
如若转载,请注明出处:http://www.ennova-tcm.com/product/5.html
更新时间:2026-05-28 02:30:31